米FDA:Total Product Life Cycle Advisory Program (TAP)について
トータル・プロダクト・ライフサイクル・アドバイザリー・プログラムは、ブレイクスルー指定された製品を、今までよりも、より早く患者さんの手元に届け、患者さんが革新的技術の恩恵を受けられるようにすることを目的として、2024年1月から始まりました。これは、ブレイクスルー指定を受けている製品のうち、プレサブミッションなどFDAとの正式なコミュニケーションを未だとっていない製品が対象となっています。
このプログラムに申請し選ばれると、専任のTAPアドバイザー、OPEQ(製品評価品質部門:Office of Product Evaluation and Quality)の審査スタッフ、CDRH(医療機器・放射線保健センター:Center for Devices and Radiological Health)の担当部署の専門家からの、積極的な、解決策を重視した取り組みが得られます。
また、個々の相談事項について、専任のTAPアドバイザーに連絡をとると、14日以内にミーティングができるほか、必要や希望に応じ、TAPアドバイザーを通じて患者団体、医療団体、医療保険会社などの意見を聞く機会も設けることができます。
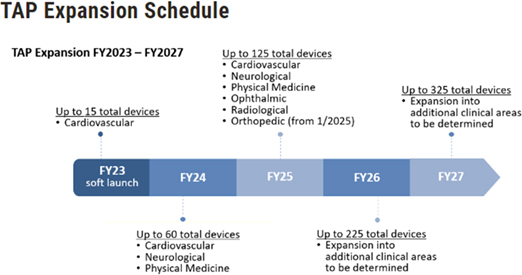
TAPプログラムは、2024年1月の開始時には循環器科領域の医療機器のみを対象としていましたが、2024年10月からは放射線科と眼科領域の機器を、2025年1月には整形外科領域の機器も対象とすることを発表しました。その他の部門の機器も順次以下の通り、申請が受け付けられる予定です。
- 2024年度:循環器科、神経科の身体医療機器を合計60製品まで受け付ける。
- 2025年度:循環器科、神経科の身体医療機器、眼科、放射線科、整形外科の医療機器を合計125製品まで受け付ける。
- 2026年度:その他の領域の製品を含め合計225製品まで受け付ける。
- 2027年度:さらに合計で325製品まで受け付ける。
グロービッツはブレークスループログラムや今回追加されたTAPにも対応できるフルコンサルティング会社です。それぞれの分野別の専門家が在籍しているため、社内で対処できることを強みとしています。アメリカ医療機器市場参入のご相談はグロービッツにお問い合わせください。
参照:米国食品医薬品局 "Total Product Life Cycle Advisory Program (TAP) | FDA"

